
విషయము
ఇతర విభాగాలుకెమిస్ట్రీలో, వాలెన్స్ ఎలక్ట్రాన్లు ఒక మూలకం యొక్క వెలుపలి ఎలక్ట్రాన్ షెల్లో ఉన్న ఎలక్ట్రాన్లు. ఒక నిర్దిష్ట అణువులోని వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను ఎలా కనుగొనాలో తెలుసుకోవడం రసాయన శాస్త్రవేత్తలకు ఒక ముఖ్యమైన నైపుణ్యం, ఎందుకంటే ఈ సమాచారం రసాయన బంధాల రకాలను నిర్ణయిస్తుంది మరియు అందువల్ల మూలకం యొక్క రియాక్టివిటీ. అదృష్టవశాత్తూ, మీరు ఒక మూలకం యొక్క వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనవలసిందల్లా మూలకాల యొక్క ప్రామాణిక ఆవర్తన పట్టిక.
దశలు
2 యొక్క పార్ట్ 1: ఆవర్తన పట్టికతో వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం
పరివర్తన లేని లోహాలు
ఒక కనుగొనండి మూలకాల ఆవర్తన పట్టిక. ఇది మానవజాతికి తెలిసిన అన్ని రసాయన మూలకాలను జాబితా చేసే అనేక విభిన్న చతురస్రాలతో రూపొందించిన రంగు-కోడెడ్ పట్టిక. ఆవర్తన పట్టిక మూలకాల గురించి చాలా సమాచారాన్ని వెల్లడిస్తుంది - మేము పరిశీలిస్తున్న అణువులోని వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించడానికి ఈ సమాచారాన్ని కొంత ఉపయోగిస్తాము. మీరు సాధారణంగా కెమిస్ట్రీ పాఠ్యపుస్తకాల కవర్ లోపల వీటిని కనుగొనవచ్చు. ఆన్లైన్లో అద్భుతమైన ఇంటరాక్టివ్ టేబుల్ కూడా అందుబాటులో ఉంది.

1 నుండి 18 వరకు మూలకాల ఆవర్తన పట్టికలో ప్రతి నిలువు వరుసను లేబుల్ చేయండి. సాధారణంగా, ఆవర్తన పట్టికలో, ఒకే నిలువు కాలమ్లోని అన్ని అంశాలు ఒకే సంఖ్యలో వాలెన్స్ ఎలక్ట్రాన్లను కలిగి ఉంటాయి. మీ ఆవర్తన పట్టికలో ఇప్పటికే ప్రతి కాలమ్ సంఖ్య లేకపోతే, ప్రతి ఒక్కటి ఎడమ ఎడమ చివర 1 తో ప్రారంభించి, కుడి వైపున 18 తో ఇవ్వండి. శాస్త్రీయ పరంగా, ఈ నిలువు వరుసలను మూలకం అంటారు "సమూహాలు."- ఉదాహరణకు, మేము సమూహాలను లెక్కించని ఆవర్తన పట్టికతో పనిచేస్తుంటే, మేము హైడ్రోజన్ (హెచ్) పైన 1, బెరిలియం (బి) పైన 2 వ్రాస్తాము మరియు హీలియం (అతడు) పైన 18 వ్రాసే వరకు. .
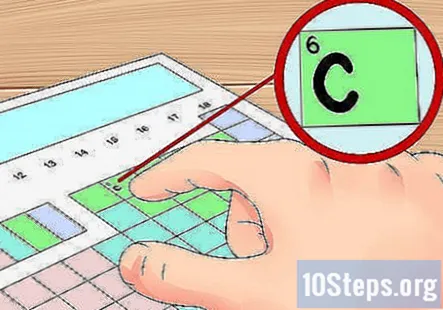
పట్టికలో మీ మూలకాన్ని కనుగొనండి. ఇప్పుడు, మీరు పట్టికలో ఉన్న వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనాలనుకునే మూలకాన్ని కనుగొనండి. మీరు దీన్ని దాని రసాయన చిహ్నం (ప్రతి పెట్టెలోని అక్షరాలు), దాని పరమాణు సంఖ్య (ప్రతి పెట్టె యొక్క ఎడమ ఎగువ భాగంలో ఉన్న సంఖ్య) లేదా పట్టికలో మీకు అందుబాటులో ఉన్న ఇతర సమాచారాలతో చేయవచ్చు.- ఉదాహరణకు ప్రయోజనాల కోసం, చాలా సాధారణ మూలకం కోసం వాలెన్స్ ఎలక్ట్రాన్లను కనుగొందాం: కార్బన్ (సి). ఈ మూలకం 6 యొక్క పరమాణు సంఖ్యను కలిగి ఉంది. ఇది సమూహం 14 పైభాగంలో ఉంది. తదుపరి దశలో, మేము దాని వాలెన్స్ ఎలక్ట్రాన్లను కనుగొంటాము.
- ఈ ఉపవిభాగంలో, సమూహాలు 3 నుండి 12 వరకు చేసిన దీర్ఘచతురస్ర ఆకారపు బ్లాక్లోని మూలకాలు అయిన పరివర్తన లోహాలను మేము విస్మరించబోతున్నాము. ఈ అంశాలు మిగతా వాటికి కొద్దిగా భిన్నంగా ఉంటాయి, కాబట్టి ఈ ఉపవిభాగంలో దశలు గెలిచాయి ' వాటిపై పని చేయవద్దు. దిగువ ఉపవిభాగంలో వీటిని ఎలా ఎదుర్కోవాలో చూడండి.
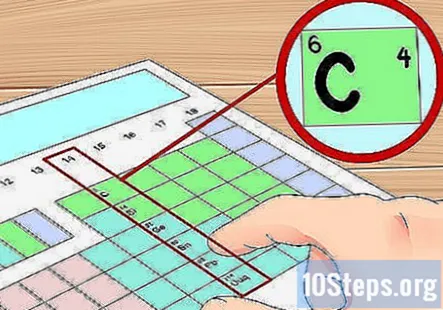
వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించడానికి సమూహ సంఖ్యలను ఉపయోగించండి. పరివర్తన రహిత లోహం యొక్క సమూహ సంఖ్య ఆ మూలకం యొక్క అణువులోని వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను కనుగొనడానికి ఉపయోగించవచ్చు. ది సమూహ సంఖ్య యొక్క స్థలం ఈ మూలకాల యొక్క అణువులోని వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్య. వేరే పదాల్లో:- సమూహం 1: 1 వాలెన్స్ ఎలక్ట్రాన్
- సమూహం 2: 2 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 13: 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 14: 4 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 15: 5 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 16: 6 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 17: 7 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 18: 8 వాలెన్స్ ఎలక్ట్రాన్లు (హీలియం మినహా, ఇది 2 కలిగి ఉంది)
- మా ఉదాహరణలో, కార్బన్ 14 వ సమూహంలో ఉన్నందున, కార్బన్ యొక్క ఒక అణువు ఉందని మేము చెప్పగలం నాలుగు వాలెన్స్ ఎలక్ట్రాన్లు.
పరివర్తన లోహాలు
గుంపులు 3 నుండి 12 వరకు ఒక మూలకాన్ని కనుగొనండి. పైన చెప్పినట్లుగా, 3 నుండి 12 సమూహాలలోని మూలకాలను "పరివర్తన లోహాలు" అని పిలుస్తారు మరియు వాలెన్స్ ఎలక్ట్రాన్ల విషయానికి వస్తే మిగిలిన మూలకాల కంటే భిన్నంగా ప్రవర్తిస్తాయి. ఈ విభాగంలో, ఈ అణువులకు వాలెన్స్ ఎలక్ట్రాన్లను కేటాయించడం కొంతవరకు సాధ్యం కాదని మేము వివరిస్తాము.
- ఉదాహరణకు ప్రయోజనాల కోసం, టాంటలం (టా), మూలకం 73 ను ఎంచుకుందాం. తరువాతి కొన్ని దశల్లో, మేము దాని వాలెన్స్ ఎలక్ట్రాన్లను కనుగొంటాము (లేదా, కనీసం, ప్రయత్నించండి నుండి.)
- పరివర్తన లోహాలలో లాంతనైడ్ మరియు ఆక్టినైడ్ సిరీస్ ("అరుదైన భూమి లోహాలు" అని కూడా పిలుస్తారు) ఉన్నాయి - రెండు వరుసల మూలకాలు సాధారణంగా లాంతనం మరియు ఆక్టినియంతో ప్రారంభమయ్యే మిగిలిన పట్టిక క్రింద ఉంచబడతాయి. ఈ అంశాలు అన్నీ చెందినవి సమూహం 3 ఆవర్తన పట్టిక.
పరివర్తన లోహాలకు "సాంప్రదాయ" వాలెన్స్ ఎలక్ట్రాన్లు లేవని అర్థం చేసుకోండి. పరివర్తన లోహాలు మిగతా ఆవర్తన పట్టిక మాదిరిగా ఎందుకు "పని చేయవు" అని అర్థం చేసుకోవటానికి అణువులలో ఎలక్ట్రాన్లు ప్రవర్తించే విధానం గురించి కొద్దిగా వివరణ అవసరం. త్వరితగతిన అమలు చేయడానికి క్రింద చూడండి లేదా సమాధానాలను సరిగ్గా పొందడానికి ఈ దశను దాటవేయండి.
- ఒక అణువుకు ఎలక్ట్రాన్లు జతచేయబడినప్పుడు, అవి వేర్వేరు "కక్ష్యలు" గా క్రమబద్ధీకరించబడతాయి - ప్రాథమికంగా ఎలక్ట్రాన్లు సమావేశమయ్యే కేంద్రకం చుట్టూ వేర్వేరు ప్రాంతాలు. సాధారణంగా, వాలెన్స్ ఎలక్ట్రాన్లు బయటి షెల్లోని ఎలక్ట్రాన్లు - మరో మాటలో చెప్పాలంటే, చివరి ఎలక్ట్రాన్లు జోడించబడ్డాయి .
- ఎలక్ట్రాన్లు బయటికి జోడించినప్పుడు ఇక్కడ వివరించడానికి కొంచెం క్లిష్టంగా ఉన్న కారణాల వల్ల d పరివర్తన లోహం యొక్క షెల్ (దీనిపై ఎక్కువ), షెల్లోకి వెళ్ళే మొదటి ఎలక్ట్రాన్లు సాధారణ వాలెన్స్ ఎలక్ట్రాన్ల వలె పనిచేస్తాయి, కానీ ఆ తరువాత, అవి చేయవు, మరియు ఇతర కక్ష్య పొరల నుండి ఎలక్ట్రాన్లు కొన్నిసార్లు బదులుగా వాలెన్స్ ఎలక్ట్రాన్లుగా పనిచేస్తాయి. దీని అర్థం, ఒక అణువు ఎలా అవకతవకలు చేయబడుతుందో దాన్ని బట్టి బహుళ సంఖ్యలో వాలెన్స్ ఎలక్ట్రాన్లను కలిగి ఉంటుంది.
సమూహ సంఖ్య ఆధారంగా వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించండి. మరోసారి, మీరు పరిశీలిస్తున్న మూలకం యొక్క సమూహ సంఖ్య దాని వాలెన్స్ ఎలక్ట్రాన్లను మీకు తెలియజేస్తుంది. ఏదేమైనా, పరివర్తన లోహాల కోసం, మీరు అనుసరించగల నమూనా లేదు - సమూహ సంఖ్య సాధారణంగా వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యకు అనుగుణంగా ఉంటుంది. ఇవి: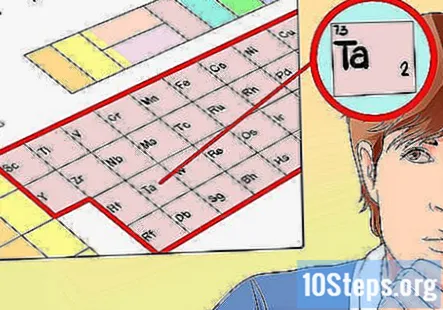
- సమూహం 3: 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 4: 2 నుండి 4 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 5: 2 నుండి 5 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 6: 2 నుండి 6 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 7: 2 నుండి 7 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 8: 2 లేదా 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 9: 2 లేదా 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 10: 2 లేదా 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 11: 1 లేదా 2 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 12: 2 వాలెన్స్ ఎలక్ట్రాన్లు
- మా ఉదాహరణలో, టాంటాలమ్ 5 వ సమూహంలో ఉన్నందున, దాని మధ్య ఉందని మేము చెప్పగలం రెండు మరియు ఐదు వాలెన్స్ ఎలక్ట్రాన్లు, పరిస్థితిని బట్టి.
పార్ట్ 2 యొక్క 2: ఎలక్ట్రాన్ కాన్ఫిగరేషన్తో వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం
ఎలక్ట్రాన్ కాన్ఫిగరేషన్ ఎలా చదవాలో తెలుసుకోండి. మూలకం యొక్క వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనటానికి మరొక మార్గం ఎలక్ట్రాన్ కాన్ఫిగరేషన్ అని పిలుస్తారు. ఇవి మొదట సంక్లిష్టంగా అనిపించవచ్చు, కానీ అవి అక్షరాలు మరియు సంఖ్యలతో అణువులోని ఎలక్ట్రాన్ కక్ష్యలను సూచించే మార్గం మరియు మీరు ఏమి చూస్తున్నారో తెలిస్తే అవి సులభం.
- మూలకం సోడియం (Na) కోసం ఉదాహరణ కాన్ఫిగరేషన్ను చూద్దాం:
- 1s2s2p3s
- ఈ ఎలక్ట్రాన్ కాన్ఫిగరేషన్ ఇలాగే పునరావృతమయ్యే స్ట్రింగ్ అని గమనించండి:
- (సంఖ్య) (అక్షరం) (సంఖ్య) (అక్షరం) ...
- ... మరియు అందువలన న. ది (సంఖ్య) (లేఖ) భాగం అనేది ఎలక్ట్రాన్ కక్ష్య యొక్క పేరు మరియు ఆ కక్ష్యలోని ఎలక్ట్రాన్ల సంఖ్య - అది అంతే!
- కాబట్టి, మా ఉదాహరణ కోసం, సోడియం ఉందని మేము చెబుతాము 1 సె కక్ష్యలో 2 ఎలక్ట్రాన్లు ప్లస్ 2s కక్ష్యలో 2 ఎలక్ట్రాన్లు ప్లస్ 2 పి కక్ష్యలో 6 ఎలక్ట్రాన్లు ప్లస్ 3s కక్ష్యలో 1 ఎలక్ట్రాన్. మొత్తం 11 ఎలక్ట్రాన్లు - సోడియం మూలకం సంఖ్య 11, కాబట్టి ఇది అర్ధమే.
- ప్రతి సబ్షెల్కు ఒక నిర్దిష్ట ఎలక్ట్రాన్ సామర్థ్యం ఉందని గుర్తుంచుకోండి. వాటి ఎలక్ట్రాన్ సామర్థ్యాలు క్రింది విధంగా ఉన్నాయి:
- s: 2 ఎలక్ట్రాన్ సామర్థ్యం
- p: 6 ఎలక్ట్రాన్ సామర్థ్యం
- d: 10 ఎలక్ట్రాన్ సామర్థ్యం
- f: 14 ఎలక్ట్రాన్ సామర్థ్యం
- మూలకం సోడియం (Na) కోసం ఉదాహరణ కాన్ఫిగరేషన్ను చూద్దాం:
మీరు పరిశీలిస్తున్న మూలకం కోసం ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను కనుగొనండి. ఒక మూలకం యొక్క ఎలక్ట్రాన్ కాన్ఫిగరేషన్ మీకు తెలిస్తే, దాని వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను కనుగొనడం చాలా సులభం (తప్ప, పరివర్తన లోహాల కోసం తప్ప.) మీకు వెళ్ళేటప్పటి నుండి కాన్ఫిగరేషన్ ఇస్తే, మీరు తదుపరి దశకు వెళ్ళవచ్చు. మీరు దానిని మీరే కనుగొనవలసి వస్తే, క్రింద చూడండి:
- ఆవర్తన పట్టికలోని చివరి మూలకం అయిన ఓగనెస్సన్ (Og), మూలకం 118 కోసం పూర్తి ఎలక్ట్రాన్ ఆకృతీకరణను పరిశీలించండి. ఇది ఏదైనా మూలకం యొక్క ఎక్కువ ఎలక్ట్రాన్లను కలిగి ఉంటుంది, కాబట్టి దాని ఎలక్ట్రాన్ కాన్ఫిగరేషన్ ఇతర మూలకాలలో మీరు ఎదుర్కొనే అన్ని అవకాశాలను ప్రదర్శిస్తుంది:
- 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d7p
- ఇప్పుడు మీకు ఇది ఉంది, మరొక అణువు యొక్క ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను కనుగొనడానికి మీరు చేయాల్సిందల్లా మీరు ఎలక్ట్రాన్ల నుండి అయిపోయే వరకు మొదటి నుండి ఈ నమూనాను పూరించండి. ఇది ధ్వనించేదానికన్నా సులభం. ఉదాహరణకు, మేము 17 ఎలక్ట్రాన్లను కలిగి ఉన్న క్లోరిన్ (Cl), ఎలిమెంట్ 17 కోసం కక్ష్య రేఖాచిత్రాన్ని తయారు చేయాలనుకుంటే, మేము దీన్ని ఇలా చేస్తాము:
- 1s2s2p3s3p
- ఎలక్ట్రాన్ల సంఖ్య 17: 2 + 2 + 6 + 2 + 5 = 17 వరకు జతచేస్తుందని గమనించండి. మీరు తుది కక్ష్యలో మాత్రమే సంఖ్యను మార్చాలి - చివరిది ముందు కక్ష్యలు పూర్తిగా నిండినందున మిగిలినవి ఒకే విధంగా ఉంటాయి .
- ఎలక్ట్రాన్ కాన్ఫిగరేషన్ల గురించి మరింత తెలుసుకోవడానికి, ఈ కథనాన్ని కూడా చూడండి.
- ఆవర్తన పట్టికలోని చివరి మూలకం అయిన ఓగనెస్సన్ (Og), మూలకం 118 కోసం పూర్తి ఎలక్ట్రాన్ ఆకృతీకరణను పరిశీలించండి. ఇది ఏదైనా మూలకం యొక్క ఎక్కువ ఎలక్ట్రాన్లను కలిగి ఉంటుంది, కాబట్టి దాని ఎలక్ట్రాన్ కాన్ఫిగరేషన్ ఇతర మూలకాలలో మీరు ఎదుర్కొనే అన్ని అవకాశాలను ప్రదర్శిస్తుంది:
ఆక్టేట్ నిబంధనతో కక్ష్య షెల్స్కు ఎలక్ట్రాన్లను కేటాయించండి. ఒక అణువుకు ఎలక్ట్రాన్లు జతచేయబడినప్పుడు, అవి పైన ఇచ్చిన క్రమం ప్రకారం వివిధ కక్ష్యలలోకి వస్తాయి - మొదటి రెండు 1 సె కక్ష్యలోకి వెళతాయి, ఆ తరువాత రెండు 2s కక్ష్యలోకి వెళతాయి, ఆ తరువాత ఆరు 2p కక్ష్యలోకి వెళుతుంది, మరియు కాబట్టి. మేము పరివర్తన లోహాల వెలుపల ఉన్న అణువులతో వ్యవహరిస్తున్నప్పుడు, ఈ కక్ష్యలు కేంద్రకం చుట్టూ "కక్ష్య గుండ్లు" గా ఏర్పడతాయని మేము చెప్తున్నాము, ప్రతి వరుస షెల్ మునుపటి వాటి కంటే ఎక్కువగా ఉంటుంది. రెండు ఎలక్ట్రాన్లను మాత్రమే కలిగి ఉన్న మొట్టమొదటి షెల్ కాకుండా, ప్రతి షెల్ ఎనిమిది ఎలక్ట్రాన్లను కలిగి ఉంటుంది (పరివర్తన లోహాలతో వ్యవహరించేటప్పుడు తప్ప, మళ్ళీ.) దీనిని అంటారు ఆక్టేట్ రూల్.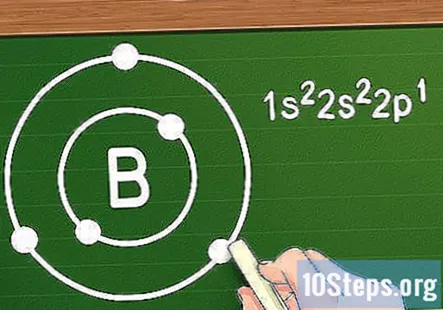
- ఉదాహరణకు, మేము బోరాన్ (బి) మూలకాన్ని చూస్తున్నామని చెప్పండి. దాని పరమాణు సంఖ్య ఐదు కాబట్టి, దీనికి ఐదు ఎలక్ట్రాన్లు ఉన్నాయని మాకు తెలుసు మరియు దాని ఎలక్ట్రాన్ కాన్ఫిగరేషన్ ఇలా కనిపిస్తుంది: 1s2s2p. మొదటి కక్ష్య షెల్లో రెండు ఎలక్ట్రాన్లు మాత్రమే ఉన్నందున, బోరాన్కు రెండు గుండ్లు ఉన్నాయని మనకు తెలుసు: ఒకటి రెండు 1 సె ఎలక్ట్రాన్లు మరియు ఒకటి 2 మరియు 2 పి కక్ష్యల నుండి మూడు ఎలక్ట్రాన్లతో.
- మరొక ఉదాహరణగా, క్లోరిన్ (1s2s2p3s3p) వంటి మూలకం మూడు కక్ష్య గుండ్లు కలిగి ఉంటుంది: ఒకటి రెండు 1s ఎలక్ట్రాన్లు, ఒకటి రెండు 2s ఎలక్ట్రాన్లు మరియు ఆరు 2p ఎలక్ట్రాన్లు, మరియు ఒకటి రెండు 3s ఎలక్ట్రాన్లు మరియు ఐదు 3p ఎలక్ట్రాన్లు.
బయటి షెల్లో ఎలక్ట్రాన్ల సంఖ్యను కనుగొనండి. ఇప్పుడు మీ మూలకం యొక్క ఎలక్ట్రాన్ గుండ్లు మీకు తెలుసు, వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం సులభం: బయటి షెల్లోని ఎలక్ట్రాన్ల సంఖ్యను ఉపయోగించండి. బయటి షెల్ నిండి ఉంటే (మరో మాటలో చెప్పాలంటే, దీనికి ఎనిమిది ఎలక్ట్రాన్లు ఉంటే లేదా, మొదటి షెల్ కోసం, రెండు), మూలకం జడంగా ఉంటుంది మరియు ఇతర మూలకాలతో సులభంగా స్పందించదు. అయితే, మరలా, పరివర్తన లోహాల కోసం విషయాలు ఈ నియమాలను పాటించవు.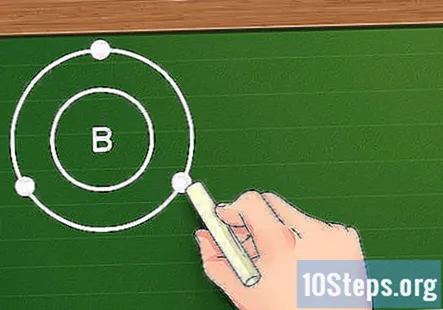
- ఉదాహరణకు, మేము బోరాన్తో కలిసి పనిచేస్తుంటే, రెండవ షెల్లో మూడు ఎలక్ట్రాన్లు ఉన్నందున, బోరాన్ ఉందని మేము చెప్పగలం మూడు వాలెన్స్ ఎలక్ట్రాన్లు.
పట్టిక యొక్క వరుసలను కక్ష్య షెల్ సత్వరమార్గాలుగా ఉపయోగించండి. ఆవర్తన పట్టిక యొక్క క్షితిజ సమాంతర వరుసలను మూలకం అంటారు "కాలాలు." పట్టిక ఎగువ నుండి మొదలుకొని, ప్రతి కాలం సంఖ్యకు అనుగుణంగా ఉంటుంది ఎలక్ట్రాన్ గుండ్లు కాలంలోని అణువులను కలిగి ఉంటుంది. ఒక మూలకం ఎన్ని వాలెన్స్ ఎలక్ట్రాన్లను కలిగి ఉందో తెలుసుకోవడానికి మీరు దీన్ని సత్వరమార్గంగా ఉపయోగించవచ్చు - ఎలక్ట్రాన్లను లెక్కించేటప్పుడు దాని కాలం యొక్క ఎడమ వైపు నుండి ప్రారంభించండి. మరోసారి, మీరు 3-12 సమూహాలను కలిగి ఉన్న ఈ పద్ధతిలో పరివర్తన లోహాలను విస్మరించాలనుకుంటున్నారు.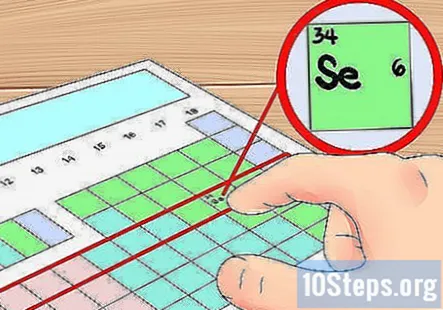
- ఉదాహరణకు, సెలీనియం మూలకం నాలుగు కక్ష్య గుండ్లు కలిగి ఉందని మనకు తెలుసు ఎందుకంటే ఇది నాల్గవ కాలంలో ఉంది. ఇది నాల్గవ కాలంలో ఎడమ నుండి ఆరవ మూలకం కనుక (పరివర్తన లోహాలను విస్మరించి), బయటి నాల్గవ షెల్లో ఆరు ఎలక్ట్రాన్లు ఉన్నాయని మనకు తెలుసు, అందువల్ల సెలీనియం కలిగి ఉంది ఆరు వాలెన్స్ ఎలక్ట్రాన్లు.
సంఘం ప్రశ్నలు మరియు సమాధానాలు
వాలెన్స్ ఎలక్ట్రాన్ను ఎలా లెక్కించాలి?
మూలకాల యొక్క ఎలక్ట్రానిక్ కాన్ఫిగరేషన్లను నిర్ణయించడం ద్వారా వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనవచ్చు. ఆ తరువాత బయటి షెల్లోని ఎలక్ట్రాన్ల సంఖ్య ఆ మూలకంలో మొత్తం వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను ఇస్తుంది.
ఒక అణువులో 33 ఎలక్ట్రాన్లు ఉంటే, ఎన్ని వాలెన్స్ ఎలక్ట్రాన్లు ఉన్నాయి?
అణువు అయాన్ కాకపోతే, అణువుకు 33 ప్రోటాన్లు ఉన్నాయని చెప్పగలను. దీని అర్థం ఇది మూలకం 33, ఇది ఆర్సెనిక్. అది పరివర్తన లోహం కాదని మనకు తెలుసు, కాబట్టి దాని సమూహ సంఖ్య యొక్క యూనిట్ అంకె 5 అని చూస్తాము, అంటే దీనికి 5 వాలెన్స్ ఎలక్ట్రాన్లు ఉన్నాయి.
హీలియం యొక్క పరమాణు సంఖ్యను నేను ఎలా నిర్ణయించగలను?
ప్రోటాన్ల సంఖ్య పరమాణు సంఖ్యకు సమానం.
ఎలక్ట్రాన్లు పాజిటివ్ చార్జ్ కాకుండా నెగటివ్ చార్జ్ ఎందుకు పొందుతాయి?
అణువులు ఎలక్ట్రాన్లను, ప్రతికూల చార్జీలను పొందుతాయి లేదా కోల్పోతాయి, ఎందుకంటే ప్రోటాన్లు సానుకూల చార్జ్ కలిగి ఉంటాయి మరియు అవి కేంద్రకంలో బలమైన అణుశక్తితో ఉంటాయి. విశ్వంలోని నాలుగు విభిన్న శక్తులలో ఇది ఒకటి: గురుత్వాకర్షణ, విద్యుదయస్కాంతత్వం, బలహీనమైన శక్తి మరియు బలమైన అణుశక్తి. ప్రోటాన్లు ఒకదానికొకటి తిప్పికొట్టేటప్పటికి అవి బలంగా ఉండాలి, అయితే అవి న్యూక్లియస్లో నిజంగా దగ్గరగా ఉంటాయి (న్యూట్రాన్లతో పాటు, బలమైన శక్తి కూడా కలిగి ఉంటాయి.) ఆలోచన ఏమిటంటే, బలమైన శక్తి చాలా బలంగా ఉంటుంది, కానీ చాలా తక్కువ దూరాలకు మాత్రమే. చిన్న సూపర్ స్ట్రాంగ్ హుక్స్ ఆలోచించండి. ప్రోటాన్లు మరియు న్యూట్రాన్లను హుక్ అప్ చేయడానికి, మీకు నక్షత్రం, సూపర్నోవా లేదా అణు పేలుడు యొక్క అపారమైన గురుత్వాకర్షణ వంటి శక్తులు అవసరం.
నోబెల్ వాయువుల వాలెన్స్ ఎలక్ట్రాన్ ఏమిటి?
నోబెల్ వాయువులు ఎనిమిది వాలెన్స్ ఎలక్ట్రాన్లను కలిగి ఉంటాయి - ఒక మూలకానికి అత్యంత స్థిరమైన స్థితి.
నత్రజనికి 6 వాలెన్స్ ఎలక్ట్రాన్లు ఎందుకు ఉన్నాయి, కానీ ఇది 15 వ సమూహంలో ఉంది?
నత్రజని ఐదు వాలెన్స్ ఎలక్ట్రాన్లను మాత్రమే కలిగి ఉంది, ఎందుకంటే ఇది గ్రూప్ 5 లో ఉంది, వాస్తవానికి ఇది గ్రూప్ 15 లో ఉన్నప్పటికీ మీరు పరివర్తన లోహాలను విస్మరించబోతున్నారు ఎందుకంటే ఈ సమూహాలకు వాటి వాలెన్స్ ఎలక్ట్రాన్లను నిర్ణయించడానికి వివిధ మార్గాలు ఉన్నాయి. అందువల్ల: గ్రూప్ 13 అంటే గ్రూప్ 3 కాబట్టి మొదలగునవి.
ఒక అణువులో 7 ప్రోటాన్లు, 8 న్యూరాన్లు మరియు 7 ఎలక్ట్రాన్లు ఉన్నాయి. దాని వాలెన్స్ షెల్లోని ఎలక్ట్రాన్ల సంఖ్య ఎంత?
7 ప్రోటాన్లు కలిగిన మూలకం నత్రజని. నత్రజని వాలెన్స్ షెల్లో 5 ఎలక్ట్రాన్లను కలిగి ఉన్న మూలకాల కాలమ్లో ఉంటుంది. ఒక నిర్దిష్ట మూలకంలో వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను కనుగొనటానికి న్యూట్రాన్ల సంఖ్య అసంబద్ధం.
ఆవర్తన పట్టికలో ఏడు బాహ్య షెల్ ఎలక్ట్రాన్లతో అణువులు ఎక్కడ ఉన్నాయి?
జడ వాయువుల పక్కన, కుడి వైపున రెండవ నుండి చివరి కాలమ్లో చూడండి.
వాలెన్స్ ఎలక్ట్రాన్ అంటే ఏమిటి?
ఒక వాలెన్స్ ఎలక్ట్రాన్ ఒక ఎలక్ట్రాన్, ఇది అణువు యొక్క వెలుపలి భాగంలో కనుగొనబడుతుంది మరియు దానిని ప్రతిచర్యలో పంచుకోవచ్చు లేదా తీసుకోవచ్చు.
ఆవర్తన పట్టికలోని మూలకాలకు వేర్వేరు సంఖ్యల వాలెన్స్ ఎలక్ట్రాన్లు ఎందుకు ఉన్నాయి?
అవి వేర్వేరు రసాయన నిర్మాణాలను కలిగి ఉంటాయి. రసాయన ప్రతిచర్యలను సృష్టించేది వాలెన్స్ ఎలక్ట్రాన్లు.
చిట్కాలు
- కాన్ఫిగరేషన్ ప్రారంభంలో కక్ష్యల కొరకు నిలబడటానికి నోబెల్ వాయువులను (సమూహం 18 లోని మూలకాలు) ఉపయోగించడం ద్వారా ఎలక్ట్రాన్ కాన్ఫిగరేషన్లను ఒక విధమైన సంక్షిప్తలిపిలో వ్రాయవచ్చని గమనించండి. ఉదాహరణకు, సోడియం యొక్క ఎలక్ట్రాన్ కాన్ఫిగరేషన్ 3s1 అని వ్రాయవచ్చు - ముఖ్యంగా, ఇది నియాన్ మాదిరిగానే ఉంటుంది, కానీ 3s కక్ష్యలో మరో ఎలక్ట్రాన్తో ఉంటుంది.
- పరివర్తన లోహాలు పూర్తిగా నింపని వాలెన్స్ సబ్షెల్లను కలిగి ఉండవచ్చు. పరివర్తన లోహాలలో వాలెన్స్ ఎలక్ట్రాన్ల యొక్క ఖచ్చితమైన సంఖ్యను నిర్ణయించడం ఈ వ్యాసం యొక్క పరిధికి మించిన క్వాంటం సిద్ధాంతం యొక్క సూత్రాలను కలిగి ఉంటుంది.
- ఆవర్తన పట్టికలు దేశానికి దేశానికి భిన్నంగా ఉంటాయని గమనించండి. కాబట్టి, గందరగోళాన్ని నివారించడానికి మీరు సరైన, నవీకరించబడినదాన్ని ఉపయోగిస్తున్నారో లేదో తనిఖీ చేయండి.
- వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం కోసం చివరి కక్ష్య నుండి ఎప్పుడు జోడించాలో లేదా తీసివేయాలో తెలుసుకోండి.
మీకు కావాల్సిన విషయాలు
- మూలకాల ఆవర్తన పట్టిక
- పెన్సిల్
- పేపర్
వికీలో ప్రతిరోజూ, మీకు మంచి జీవితాన్ని గడపడానికి సహాయపడే సూచనలు మరియు సమాచారానికి ప్రాప్యత ఇవ్వడానికి మేము తీవ్రంగా కృషి చేస్తాము, అది మిమ్మల్ని సురక్షితంగా, ఆరోగ్యంగా లేదా మీ శ్రేయస్సును మెరుగుపరుస్తుంది. ప్రస్తుత ప్రజారోగ్యం మరియు ఆర్థిక సంక్షోభాల మధ్య, ప్రపంచం ఒక్కసారిగా మారిపోతున్నప్పుడు మరియు మనమందరం రోజువారీ జీవితంలో మార్పులను నేర్చుకుంటూ, అలవాటు పడుతున్నప్పుడు, ప్రజలకు గతంలో కంటే వికీ అవసరం. మీ మద్దతు వికీకి మరింత లోతైన ఇలస్ట్రేటెడ్ కథనాలు మరియు వీడియోలను సృష్టించడానికి మరియు ప్రపంచవ్యాప్తంగా ఉన్న మిలియన్ల మంది వ్యక్తులతో మా విశ్వసనీయ బోధనా కంటెంట్ను పంచుకోవడానికి సహాయపడుతుంది. దయచేసి ఈ రోజు వికీకి ఎలా తోడ్పడుతుందో పరిశీలించండి.


