విషయము
- దశల్లో
- విధానం 1 ట్రయల్ మరియు ఎర్రర్ పద్ధతి ద్వారా సమీకరణాన్ని సమతుల్యం చేయడం
- విధానం 2 బీజగణిత పద్ధతి ద్వారా సమీకరణాన్ని సమం చేయండి
రసాయన శాస్త్రంలో, ఒక రసాయన ప్రతిచర్య సమయంలో ఏమి జరిగిందో ఒక సమీకరణం నిర్ధారిస్తుంది. సమీకరణం యొక్క ఎడమ వైపున, మేము ప్రయోగానికి ఉపయోగించిన కారకాలను మరియు కుడి వైపున, ప్రయోగం సమయంలో పొందిన ఉత్పత్తులను ఉంచుతాము. రసాయన ప్రతిచర్య సమయంలో ద్రవ్యరాశి (లావోసియర్) పరిరక్షణ సూత్రం ప్రకారం, అణువు కనిపించదు, ఏదీ సృష్టించబడదు, అవి భిన్నంగా కలిసిపోతాయి. సారాంశంలో, మీరు సమీకరణం యొక్క ఎడమ వైపున ఉన్న ప్రతి మూలకం యొక్క ఒకే సంఖ్య డాటోమ్లను కలిగి ఉండాలి. అందుకే బ్యాలెన్స్ సమీకరణం ఎప్పుడూ సమతుల్యంగా ఉండాలి.
దశల్లో
విధానం 1 ట్రయల్ మరియు ఎర్రర్ పద్ధతి ద్వారా సమీకరణాన్ని సమతుల్యం చేయడం
-
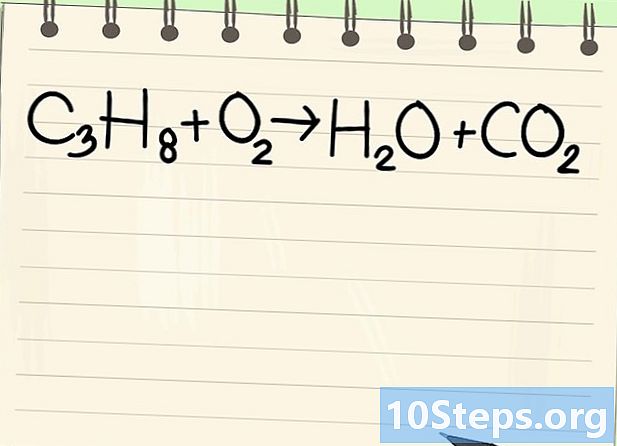
బ్యాలెన్స్ సమీకరణాన్ని గమనించండి. మేము ఈ క్రింది సమీకరణానికి చికిత్స చేస్తాము:- సి3H8 + ఓ2 -> హెచ్2O + CO2
- ఇది ప్రొపేన్ దహన సమీకరణం (సి3H8) ఆక్సిజన్లో: నీరు మరియు కార్బన్ డయాక్సైడ్ పొందబడతాయి.
-
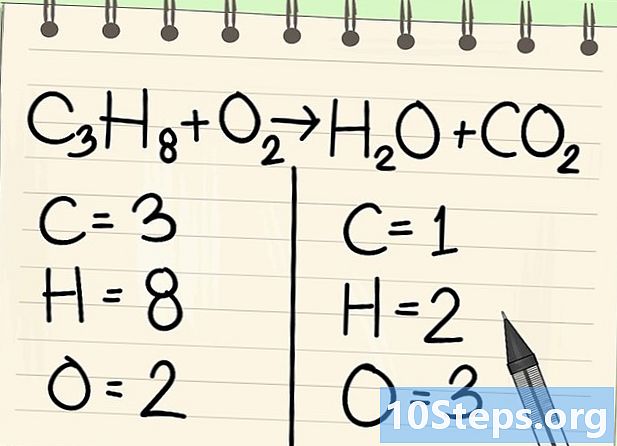
అణువులను లెక్కించండి. సమీకరణం యొక్క ఒక వైపున ప్రతి మూలకం యొక్క డాటామ్ల సంఖ్యను నమోదు చేయండి, తరువాత మరొకటి. దీని కోసం, సూచికలను పరిగణనలోకి తీసుకోండి, ఏదీ లేకపోతే, సూచిక 1.- ఎడమ వైపున, 3 కార్బన్ అణువులు, 8 హైడ్రోజన్ మరియు 2 ఆక్సిజన్ ఉన్నాయి.
- కుడి వైపున, కార్బన్ యొక్క 1 అణువు, 2 హైడ్రోజన్ మరియు 3 ఆక్సిజన్ ఉన్నాయి.
-
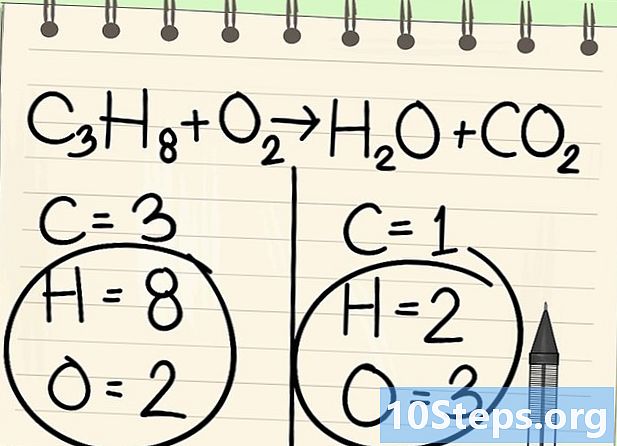
హైడ్రోజన్ మరియు ఆక్సిజన్ను కొద్దిసేపు పక్కన పెట్టండి. -

సరైన మూలకంతో బ్యాలెన్సింగ్ ప్రారంభించండి. ప్రతిచర్యకు ముందు మరియు తరువాత అణువులోని ఒకదానితో మేము ఎల్లప్పుడూ ప్రారంభిస్తాము. అనేక ఉంటే, అణువులలో ఒకదానిలో మోనోవాలెంట్ ఉన్నదాన్ని తీసుకోండి. ఇక్కడ మనం కార్బన్ అణువులతో ప్రారంభిస్తాము. -

కార్బన్ అణువులను సమతుల్యం చేయండి. కుడి వైపున, కార్బన్ డయాక్సైడ్ అణువు (CO) కు గుణకం జోడించండి2) దీనిలో కార్బన్ లాటోమ్ ఒంటరిగా ఉంటుంది. 3 ఎడమ అణువులను పొందడానికి 3 ని పెడతాము.- సి3H8 + ఓ2 -> హెచ్2O + 3CO2
- అందువల్ల మనకు 3 కార్బన్ అణువులను గుణకం (3CO) కు సరైన కృతజ్ఞతలు ఉన్నాయి2) మరియు ఎడమవైపు 3 కార్బన్ అణువులను సూచిక (సి) కు కృతజ్ఞతలు3H8).
- ఒక సమీకరణంలో, మీకు కావలసిన అన్ని గుణకాలను మీరు ఉంచవచ్చు, కానీ మీరు ఆధారాలను తాకలేరు.
-
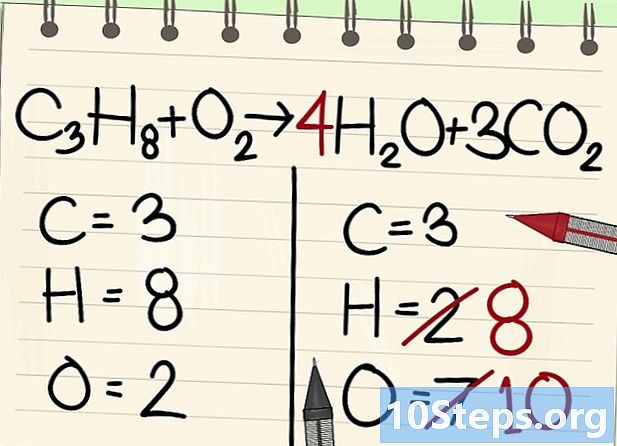
హైడ్రోజన్ అణువులను సమతుల్యం చేయండి. మీకు సమీకరణంలో 8 ఎడమ ఉన్నందున, మీకు అంత కుడి అవసరం.- సి3H8 + ఓ2 --> 4H2O + 3CO2
- కుడి వైపున, మీరు 4 యొక్క గుణకాన్ని ఉంచుతారు, ఎందుకంటే నీటి అణువులో హైడ్రోజన్ ద్విపద ఉంటుంది: సూచిక 2 రెండు హైడ్రోజన్ అణువులతో సంబంధం కలిగి ఉందని సూచిస్తుంది.
- కుడి వైపున ఉన్న హైడ్రోజన్ అణువుల సంఖ్యను పొందడానికి, మీరు గుణకం 4 ను సూచిక 2 లేదా 8 అణువుల ద్వారా గుణించాలి.
- ఆక్సిజన్ అణువుల విషయానికొస్తే, కుడి వైపున, ఇప్పుడు 3CO యొక్క మూడు అణువుల నుండి వస్తున్న ఒక వైపు 6 ఉన్నాయి2 (3 x 2 = 6 అణువులు) మరియు 4 H యొక్క 4 అణువుల నుండి 42O (4 x 1 = 4 అణువులు), అంటే మొత్తం 10 అణువుల ఆక్సిజన్.
-
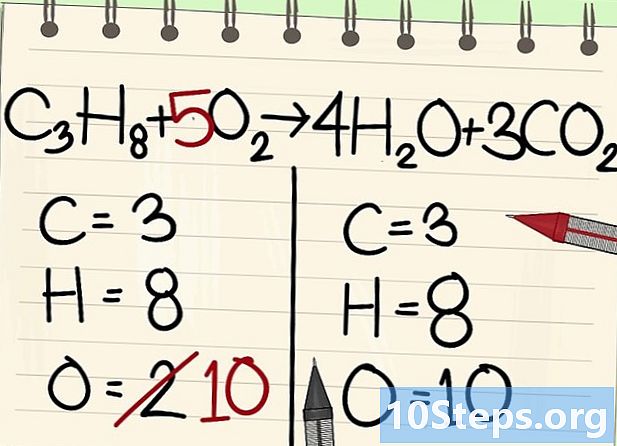
ఆక్సిజన్ యొక్క అణువులను సమతుల్యం చేయండి.- కార్బన్ మరియు హైడ్రోజన్ బ్యాలెన్స్ కారణంగా, సమీకరణం యొక్క రెండు వైపులా ఆక్సిజన్ అణువుల సంఖ్య ఒకేలా ఉండదు. కుడి వైపున 10 అణువుల ఆక్సిజన్ ఉందని మేము ఇంతకుముందు చూశాము (నీటి అణువుల నుండి 4, మరియు కార్బన్ డయాక్సైడ్ అణువుల నుండి 6). ఎడమ వైపున, 2 మాత్రమే ఉన్నాయి (O నుండి2).
- ఆక్సిజన్ను సమతుల్యం చేయడానికి, ఎడమ ఆక్సిజన్ అణువుకు 5 గుణకాన్ని జోడించండి: మీకు ఎడమవైపు 10 అణువుల ఆక్సిజన్ మరియు మరొకటి కుడి వైపున ఉంటాయి.
- సి3H8 + 5O2 -> 4 హెచ్2O + 3CO2
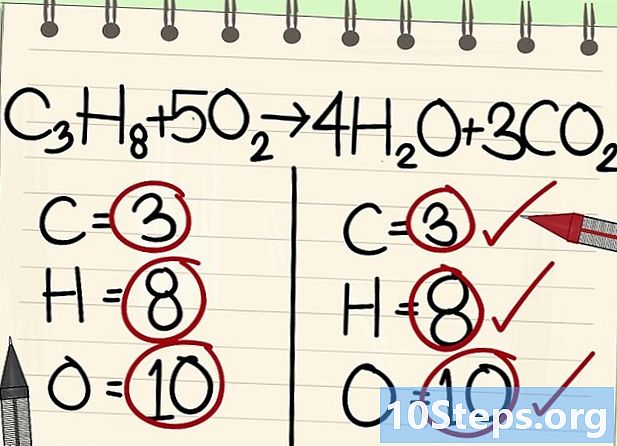
- అన్ని అణువుల (కార్బన్, హైడ్రోజన్ మరియు ఆక్సిజన్) సమతుల్యమైనవి: మీ సమీకరణం సమతుల్యమవుతుంది.
విధానం 2 బీజగణిత పద్ధతి ద్వారా సమీకరణాన్ని సమం చేయండి
-

సమతుల్యతకు సమీకరణాన్ని వ్రాయండి. ప్రతి అణువును అక్షర గుణకం కేటాయించండి. మేము వారిని పిలుస్తాము ఉంది, బి, సి మరియు d. -
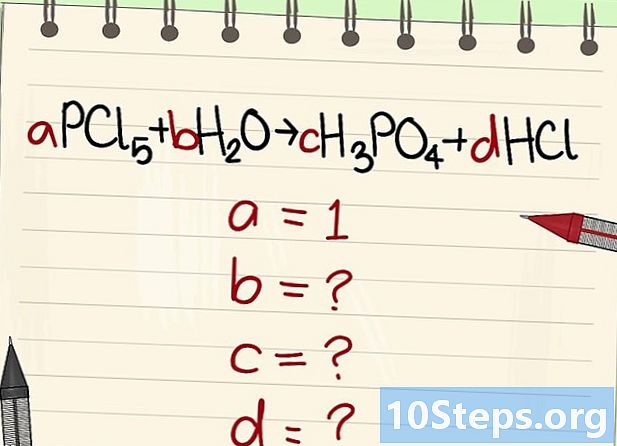
ఇతర సాహిత్య గుణకాల విలువను కనుగొనండి. మేము దానిని అడుగుతాము ఉంది = 1. -

ఈ గుణకాల మధ్య సంబంధాలను కనుగొనండి. ఎడమ (కారకాలు) మరియు కుడి (ఉత్పత్తులు) చూస్తే, ఈ విభిన్న గుణకాల మధ్య సంబంధాలను ఏర్పరచుకోండి.- కింది సమీకరణాన్ని తీసుకోండి: aPCl5 + bH2O = cH3PO4 + dHCl. A = 1, అంటే c = a, d = 5a మరియు 2b = 3c + d అని పేర్కొనబడింది. లెక్కలు పూర్తయ్యాయి, సి = 1, డి = 5 మరియు బి = 4.

- కింది సమీకరణాన్ని తీసుకోండి: aPCl5 + bH2O = cH3PO4 + dHCl. A = 1, అంటే c = a, d = 5a మరియు 2b = 3c + d అని పేర్కొనబడింది. లెక్కలు పూర్తయ్యాయి, సి = 1, డి = 5 మరియు బి = 4.