విషయము
కెమిస్ట్రీలో, విద్యుదాత్మకత ఇది ఒక అణువు ఒక బంధంలో ఎలక్ట్రాన్లపై చూపించే ఆకర్షణ యొక్క కొలత. అధిక ఎలక్ట్రోనెగటివిటీ ఉన్న అణువు ఎలక్ట్రాన్లను గొప్ప తీవ్రతతో ఆకర్షిస్తుంది, తక్కువ ఎలక్ట్రోనెగటివిటీ ఉన్న అణువు తక్కువ తీవ్రతతో చేస్తుంది. ఈ విలువలు ఒకదానితో ఒకటి బంధించినప్పుడు విభిన్న అణువులు ఎలా ప్రవర్తిస్తాయో అంచనా వేయడానికి ఉపయోగిస్తారు, ఈ అంశం ప్రాథమిక రసాయన శాస్త్రంలో ఒక ముఖ్యమైన నైపుణ్యంగా మారుతుంది.
స్టెప్స్
3 యొక్క పద్ధతి 1: ఎలక్ట్రోనెగటివిటీ యొక్క ప్రాథమిక అంశాలు
అణువులు ఎలక్ట్రాన్లను పంచుకున్నప్పుడు రసాయన బంధాలు జరుగుతాయని అర్థం చేసుకోండి. ఎలక్ట్రోనెగటివిటీని అర్థం చేసుకోవడానికి, మొదట "లింక్" అంటే ఏమిటో అర్థం చేసుకోవాలి. పరమాణు రేఖాచిత్రంలో ఒకదానితో ఒకటి "అనుసంధానించబడిన" అణువులోని ఏదైనా రెండు అణువుల మధ్య బంధం ఉందని చెబుతారు. ముఖ్యంగా, వారు రెండు ఎలక్ట్రాన్ల సమితిని పంచుకుంటారని దీని అర్థం - ప్రతి అణువు బంధానికి ఒక అణువును దోహదం చేస్తుంది.
- అణువులు ఎలక్ట్రాన్లను మరియు బంధాన్ని ఎందుకు పంచుకుంటాయనే దానిపై ఖచ్చితమైన కారణాలు ఈ వ్యాసం యొక్క దృష్టికి అనుగుణంగా లేవు. మీరు మరింత తెలుసుకోవాలనుకుంటే, రసాయన బంధాల యొక్క ప్రాథమిక భావనల కోసం ఇంటర్నెట్లో శోధించండి.
బంధంలో ఉన్న ఎలక్ట్రాన్లను ఎలక్ట్రోనెగటివిటీ ఎలా ప్రభావితం చేస్తుందో అర్థం చేసుకోండి. రెండు అణువులు ఒక బంధంలో రెండు ఎలక్ట్రాన్ల సమితిని పంచుకున్నప్పుడు, రెండింటి మధ్య సమాన భాగస్వామ్యం ఎప్పుడూ ఉండదు. వాటిలో ఒకదానితో జతచేయబడిన అణువు కంటే ఎక్కువ ఎలక్ట్రోనెగటివిటీ ఉన్నప్పుడు, అది రెండు ఎలక్ట్రాన్లను తన దగ్గరికి తీసుకువస్తుంది. చాలా ఎక్కువ ఎలెక్ట్రోనెగటివిటీ ఉన్న అణువు బంధంలో ఎలక్ట్రాన్లను దాని వైపుకు లాగగలదు, మరొకటితో పంచుకోవడాన్ని దాదాపు రద్దు చేస్తుంది.- ఉదాహరణకు, NaCl (సోడియం క్లోరైడ్) అణువులో, క్లోరిన్ అణువు అధిక ఎలక్ట్రోనెగటివిటీని కలిగి ఉంటుంది మరియు సోడియం, తక్కువ ఎలక్ట్రోనెగటివిటీని కలిగి ఉంటుంది. త్వరలో, ఎలక్ట్రాన్లు లాగబడతాయి క్లోరిన్ వైపు మరియు సోడియం నుండి దూరంగా.

ఎలక్ట్రోనెగటివిటీ పట్టికను సూచనగా ఉపయోగించండి. ఎలెక్ట్రోనెగటివిటీ పట్టిక ఆవర్తన పట్టిక వలె సరిగ్గా అమర్చబడిన అంశాలను అందిస్తుంది, కానీ ప్రతి అణువుతో దాని ఎలక్ట్రోనెగటివిటీతో లేబుల్ చేయబడుతుంది. వాటిని అనేక కెమిస్ట్రీ పాఠ్యపుస్తకాల్లో, సాంకేతిక వ్యాసాలలో మరియు ఇంటర్నెట్లో కూడా చూడవచ్చు.- ఇక్కడ అద్భుతమైన ఎలక్ట్రోనెగటివిటీ పట్టిక ఉంది. ఇది పాలింగ్ ఎలక్ట్రోనెగటివిటీ స్కేల్ను ఉపయోగిస్తుందని గమనించండి, ఇది చాలా సాధారణం. అయినప్పటికీ, ఎలక్ట్రోనెగటివిటీని కొలవడానికి ఇతర మార్గాలు ఉన్నాయి, వాటిలో ఒకటి క్రింద చూపబడుతుంది.
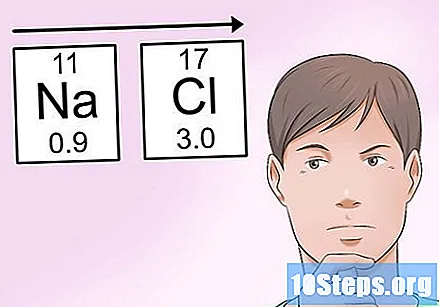
అంచనాలను సులభంగా చేయడానికి ఎలక్ట్రోనెగటివిటీ పోకడలను గుర్తుంచుకోండి. మీకు చేతిలో ఎలక్ట్రోనెగటివిటీ పట్టిక లేకపోతే, ఆవర్తన పట్టికలో మీ స్థానం ఆధారంగా ఈ విలువను అంచనా వేయడం ఇప్పటికీ సాధ్యమే. సాధారణ నియమం ప్రకారం:- అణువు యొక్క ఎలెక్ట్రోనెగటివిటీ పెరుగుతుంది మీరు వెళ్ళినప్పుడు కుడి ఆవర్తన పట్టికలో.
- అణువు యొక్క ఎలెక్ట్రోనెగటివిటీ పెరుగుతుంది మీరు వెళ్ళినప్పుడు అప్ ఆవర్తన పట్టికలో.
- అందువల్ల, ఎగువ కుడి మూలలోని అణువులలో అత్యధిక ఎలక్ట్రోనెగటివిటీ విలువలు ఉంటాయి మరియు దిగువ ఎడమ మూలలో ఉన్నవి అతి తక్కువ.
- ఉదాహరణకు, మునుపటి NaCl ఉదాహరణలో, క్లోరిన్ సోడియం కంటే ఎక్కువ ఎలక్ట్రోనెగటివిటీని కలిగి ఉందని మీరు నిర్ణయించవచ్చు ఎందుకంటే ఇది దాదాపు అత్యధిక కుడి పాయింట్ వద్ద ఉంది. మరోవైపు, సోడియం టేబుల్ యొక్క ఎడమ వైపున చాలా దూరంలో ఉంది, ఇది అతి తక్కువ విలువైన అణువులలో ఒకటిగా చేస్తుంది.
3 యొక్క విధానం 2: ఎలక్ట్రోనెగటివిటీతో కనెక్షన్లను కనుగొనడం
రెండు అణువుల మధ్య ఎలక్ట్రోనెగటివిటీలో వ్యత్యాసాన్ని కనుగొనండి. రెండు అణువులను ఒకదానితో ఒకటి అనుసంధానించినప్పుడు, వాటి ఎలక్ట్రోనెగటివిటీ విలువల మధ్య వ్యత్యాసం ఆ బంధం యొక్క నాణ్యత గురించి చాలా తెలుపుతుంది. వ్యత్యాసాన్ని కనుగొనడానికి అతి పెద్ద నుండి అతిచిన్న విలువను తీసివేయండి.
- ఉదాహరణకు, మేము HF అణువును చూస్తున్నట్లయితే, మేము ఫ్లోరిన్ (4.0) నుండి హైడ్రోజన్ (2.1) యొక్క ఎలక్ట్రోనెగటివిటీ విలువను తీసివేస్తాము. 4.0 - 2.1 = 1,9.
వ్యత్యాసం 0.5 కన్నా తక్కువ ఉంటే, బంధం సమయోజనీయ మరియు నాన్పోలార్. ఇక్కడ, ఎలక్ట్రాన్లు దాదాపు సమాన కొలతలో పంచుకోబడతాయి. ఈ బంధాలు ఇరువైపులా చార్జ్లో పెద్ద తేడాలతో అణువులను ఏర్పరచవు. ధ్రువ బంధాలను విచ్ఛిన్నం చేయడం చాలా కష్టం.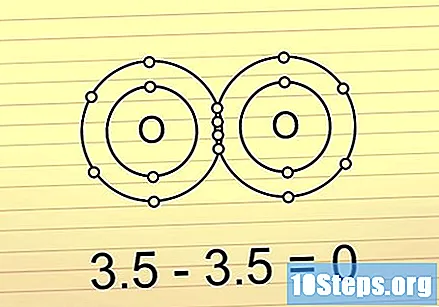
- ఉదాహరణకు, O అనే అణువు2 ఈ రకమైన కనెక్షన్ను అందిస్తుంది. రెండు ఆక్సిజన్ అణువులకు ఒకే ఎలక్ట్రోనెగటివిటీ ఉన్నందున, వాటి మధ్య వ్యత్యాసం 0 కి సమానం.
వ్యత్యాసం 0.5 మరియు 1.6 మధ్య ఉంటే, బంధం సమయోజనీయ మరియు ధ్రువంగా ఉంటుంది. ఈ బంధాలు మరొక చివర కంటే ఒక చివర ఎక్కువ ఎలక్ట్రాన్లను కలిగి ఉంటాయి. ఇది అణువును చివరలో ఎక్కువ ఎలక్ట్రాన్లతో కొంచెం ప్రతికూలంగా చేస్తుంది మరియు అవి లేకుండా చివరలో కొంచెం ఎక్కువ సానుకూలంగా ఉంటుంది. ఈ బంధాలలో ఛార్జ్ అసమతుల్యత అణువులను కొన్ని నిర్దిష్ట ప్రతిచర్యలలో పాల్గొనడానికి అనుమతిస్తుంది.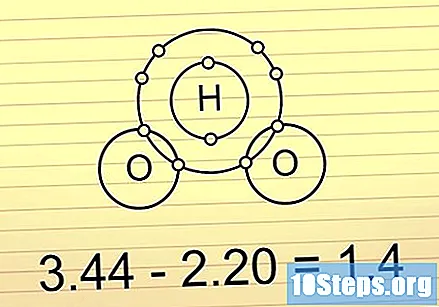
- దీనికి మంచి ఉదాహరణ H అణువు2ఓ (నీరు). O రెండు H ల కంటే ఎక్కువ ఎలెక్ట్రోనిగేటివ్, కాబట్టి ఇది ఎలక్ట్రాన్లను దగ్గరగా ఉంచుతుంది మరియు మొత్తం అణువు O చివరలో పాక్షికంగా ప్రతికూలంగా ఉంటుంది మరియు H చివర్లలో పాక్షికంగా సానుకూలంగా ఉంటుంది.
వ్యత్యాసం 2 కన్నా ఎక్కువగా ఉంటే, బంధం అయాను. ఈ బంధాలలో, ఎలక్ట్రాన్లు పూర్తిగా ఒక చివరన ఉంచబడతాయి. చాలా ఎలెక్ట్రోనిగేటివ్ అణువు ప్రతికూల చార్జ్ను పొందుతుంది మరియు అతి తక్కువ ఎలక్ట్రోనిగేటివ్ అణువు సానుకూల చార్జ్ను పొందుతుంది. ఈ రకమైన బంధం అణువులను ఇతర అణువులతో చర్య తీసుకోవడానికి లేదా, ఇంకా, ధ్రువ అణువులతో వేరు చేయడానికి అనుమతిస్తుంది.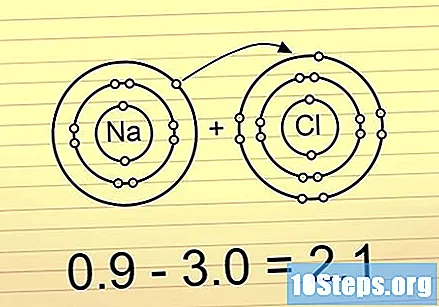
- దీనికి ఉదాహరణ NaCl (సోడియం క్లోరైడ్). క్లోరిన్ చాలా ఎలెక్ట్రోనిగేటివ్, ఇది రెండు ఎలక్ట్రాన్లను బంధం నుండి ఒకదానికొకటి లాగుతుంది, సోడియంను ధనాత్మక చార్జ్తో వదిలివేస్తుంది.
వ్యత్యాసం 1.6 మరియు 2 మధ్య ఉంటే, ఒక లోహం కోసం చూడండి. ఉంటే అక్కడ బంధంలో ఉన్న ఒక లోహం, ఇది అని సూచిస్తుంది అయాను. ఇతర లోహాలు లేనివి ఉంటే, బంధం ధ్రువ సమయోజనీయ.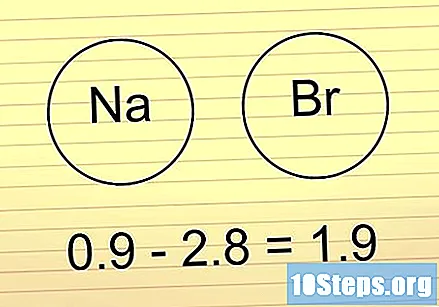
- లోహాలు ఎడమ మరియు ఆవర్తన పట్టిక మధ్యలో చాలా అణువులను కలిగి ఉంటాయి. ఈ పేజీలో లోహాలు ఏ అంశాలు ఉన్నాయో చూపించే పట్టిక ఉంది.
- మా మునుపటి HF ఉదాహరణ ఆ గుంపులో వస్తుంది. H మరియు F లోహాలు కానందున, బంధం ఉంటుంది ధ్రువ సమయోజనీయ.
3 యొక్క విధానం 3: ముల్లికెన్ ఎలక్ట్రోనెగటివిటీని కనుగొనండి
మీ అణువు యొక్క మొదటి అయనీకరణ శక్తిని కనుగొనండి. ముల్లికెన్ ఎలక్ట్రోనెగటివిటీ పైన ఉన్న పాలింగ్ పట్టికలో కనిపించే కొలతకు కొద్దిగా భిన్నంగా ఉంటుంది. ఇచ్చిన అణువు కోసం దాని విలువను కనుగొనడానికి, మీ మొదటి అయనీకరణ శక్తిని కనుగొనండి. అణువు ఉత్సర్గాన్ని ఒకే ఎలక్ట్రాన్గా చేయడానికి అవసరమైన శక్తి ఇది.
- ఈ విలువను బహుశా రసాయన సూచన పదార్థాలలో చూడవచ్చు. ఈ పేజీలో మీరు ఉపయోగించగల మంచి పట్టిక ఉంది (దాన్ని కనుగొనడానికి క్రిందికి స్క్రోల్ చేయండి).
- ఉదాహరణగా, లిథియం (లి) యొక్క ఎలెక్ట్రోనెగటివిటీ ఏమిటో మీరు తెలుసుకోవాలనుకుందాం. పై పేజీలోని పట్టికలో, మొదటి అయనీకరణ శక్తి సమానమని మనం చూడవచ్చు 520 kJ / mol.
అణువు యొక్క ఎలక్ట్రాన్ అనుబంధం ఏమిటో తెలుసుకోండి. ప్రతికూల అయాన్ ఏర్పడటానికి అణువుకు ఎలక్ట్రాన్ కలిపినప్పుడు పొందిన శక్తి యొక్క కొలత ఇది. మళ్ళీ, ఇది రిఫరెన్స్ మెటీరియల్లో కనుగొనవలసిన విషయం. ఈ పేజీకి ఉపయోగపడే వనరులు ఉన్నాయి.
- లిథియం యొక్క ఎలక్ట్రానిక్ అనుబంధం సమానం 60 kJ మోల్.
ముల్లికెన్ యొక్క ఎలక్ట్రోనెగటివిటీ సమీకరణాన్ని పరిష్కరించండి. KJ / mol ను శక్తి యూనిట్గా ఉపయోగిస్తున్నప్పుడు, ముల్లికెన్ యొక్క ఎలెక్ట్రోనెగటివిటీ సమీకరణాన్ని ఇలా వ్రాయవచ్చు ENMulliken = (1.97 × 10) (ఇనేను + ఇఇంకా) + 0,19. తెలిసిన డేటాను సమీకరణంలోకి చొప్పించి, EN విలువను కనుగొనండిMulliken.
- మా ఉదాహరణలో, మేము ఈ క్రింది తీర్మానానికి చేరుకుంటాము:
- ENMulliken = (1.97 × 10) (ఇనేను + ఇఇంకా) + 0,19
- ENMulliken = (1,97 × 10)(520 + 60) + 0,19
- ENMulliken = 1,143 + 0,19 = 1,333
- మా ఉదాహరణలో, మేము ఈ క్రింది తీర్మానానికి చేరుకుంటాము:
చిట్కాలు
- పాలింగ్ మరియు ముల్లికెన్ ప్రమాణాలతో పాటు, ఆల్రెడ్-రోచో, సాండర్సన్ మరియు అలెన్ వంటి ఇతర ఎలక్ట్రోనెగటివిటీ ప్రమాణాలు కూడా ఉన్నాయి. ఎలక్ట్రోనెగటివిటీని లెక్కించడానికి వాటిలో ప్రతి దాని స్వంత సమీకరణాలు ఉన్నాయి (మరియు వాటిలో కొన్ని చాలా క్లిష్టంగా ఉంటాయి).
- విద్యుదాత్మకత కొలత యూనిట్ లేదు.